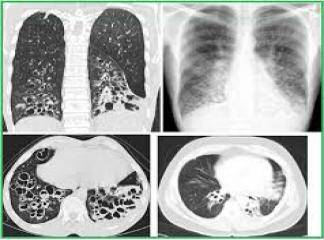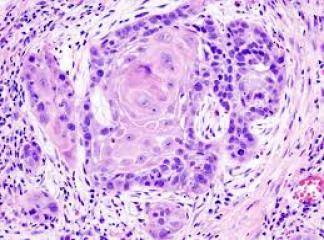
Karsinomlar
Akciğer karsinomu (akciğer kanseri) endüstrileşmiş ülkelerdeki kansere bağlı ölümlerin kuşkusuz bir numaralı sebebidir. Bu durum özellikle erkek popülasyonunda uzun zamandır böyledir ve erkeklerde kanser ölümlerinin üçte birini oluşturur. Kadınlarda da kanser ölümlerinin önemli nedenlerinden birisi haline gelmektedir.
Amerikan Kanser Derneği 2006 yılında yaklaşık 172.570 kişinin akciğer kanseri tanısı aldığını, 163.510 kişinin ise bundan öleceğini tahmin etmektedir. Erkeklerde bu orandaki artış hızı yavaşlamaktadır. Kadınlarda ise 1987' den bu yana meme kanserinden daha çok ölüme neden olan akciğer kanseri görülme oranı artmaya devam etmektedir. Bu istatistikler şüphesiz ki sigara içimi ve akciğer kanseri arasındaki nedensellik ile ilişkilidir. Akciğer kanserinin pik yaptığı yaşlar 50'li ve 60'lı yaşlardır. Tam âmâda kişilerin %50'sinden fazlasında zaten uzak metastazlar, dörtte birinde ise bölgesel lenf nodlarına metastaz vardır. Akciğer kanserinin prognozu kötüdür akciğer kanserinin tüm evreleri birlikte topluca değerlendirildiğinde 5 yıllık sağ kalım oranı %15'tir. Akciğer dışına yayılmamış olgularda bile 5 yıllık sağ kalım yaklaşık %45' tir.
Akciğer karsinomundun 4 ana histolojik tipi skuamöz hücreli karsinom, adenokarsinom, küçük hücreli karsinom ve büyük hücreli karsinomdur. Bazı olgularda histolojik paternlerde kombinasyonlar olur (örneğin kombine küçük hücreli karsinom, adenoskuamöz kaç silom). Tamamen anlaşılamayan nedenlerden dolayı, ancak olasılıkla tütün içimi şekillerindeki değişikliğe bağlı olarak son yıllarda adenokarsinom, en sık görülen primer akciğer tümörü olan skuamöz hücreli karsinom ile yer de-ğiştirmiştir. Adenokarsinom aynı zamanda kadınlarda, sigara içmeyenlerde ve 45 yaşından daha genç kişilerde en sık görülen primer akciğer tümörüdür. Her histolojik tipi ayrı tartışmadan önce akciğer tümörlerinin sınıflandırmaya temel teşkil eden bazı genel esaslan sunulmuştur.
• Terapötik amaçlara yönelik olarak, akciğer karsinomdan 2 geniş grup altında sınıflandınlmıştır: Küçük hücreli akciğer kanserleri (small-cell lung cancerSCLC) ve küçük hücreli dışı akciğer kanserleri (nonsmall-cell lung cancer-NSCLC). NSCLC grubu skuamöz hücreli, adenokarsinom ve büyük hücreli akciğer kanserlerini içerir.
• Bu ayırımda anahtar neden, hemen tüm SeLC'lerin tanı sırasında metasta; yapmış olması ve bundan dolayı cerrahi tedavi ile kiir elde edilemeyecek olmasıdır. Bu nedenle bu tip kanserler radyoterapi ile birlikte veya tek başına kemoterapi ile en uygun şekilde tedavi edilebilirler. Bunun aksine NSCLC grubu kemoterapiye yetersiz yanıt verir ve cerrahi ile daha iyi tedavi edilir.
• Morfolojik, immünofenotipik özelikler ve tedaviye yanıtta görülen farklılıklara ek olarak SCLC e NSCLC‘ LER arasında genetik farklılıklar da vardır. Örneğin, G L-S hücre siklus kontrol noktası akciğer karsinomlarının çoğunda iptal edilir. Fakat bu farklı genetik mekanizmalar aracılığı ile olur; p 16 CDKN2A geni NSCLC'larında sıklıkla in aktif iken SCLC'larında yüksek sıklıkta RE gen mutasyonlan karakteristiktir. Buna benzer olarak, KRAS aktivasyonu ve EGFR onkojen mutasyonlan neredeyse NSCLC grubunda adenokar inomlara sınırlıdır ve SCLC'larda nadirdir.
Etiyoloji ve Patogenez
Akciğer karsinomdan diğer anatomik bölgelerdeki pek çok kanserler gibi aşamalı gelişen genetik değişiklikler sonucu benign bronşial epiteline neoplastik dokuya transformasyonu ile meydana gelir. Moleküler değişikliklerin sırası gelişigüzel değildir. Kansere doğru histolojik ilerleme ile paralelolan ve önceden tahmin edilebilen bir sıra izler. Kromozom 3p de olduğu varsayılan tümör supresör gen in aktivasyonu çok erken bir olay iken, p53 mutasyonu ya da KRAS onkogen aktivasyonu nispeten daha geç meydana gelir. Daha önemlisi kromozom 3p materyal kaybı gibi genetik değişiklikler akciğer kanseri olan kişilerin kanserli alan dışı benign bronş epitellerinde görülebildiği gibi akciğer kanseri olmayan sigara içicilerinin respiratuar epitellerinde de görülür. Bu durum karsinojene maruz kalma sonucunda respiratuar epitelde geniş alanların mutasyona uğradığını göstermektedir (alan etkisi).
Bu verimli toprakta böyle hücrelerde ilave mutasyonlar gelişerek sonuçta kansere dönüşüm olur. Özellikle sigara içmeyen uzak doğulu kadınlarda görülen adenokarsinomun bir alt tipinde epiderm al büyüme faktörü reseptörü (EGFR) mutasyonunun aktivasyonu izlenir. Özellikle bu tümörler, EGFR-mutana kanser hücrelerinin aktive onkojenler bağımlı olmadan nedeni ile EGFR sinyalizasyonunu inhibe eden bir grup ajandan son derece kolay etkilenirler. Akciğer kanserinde tedaviye yol gösterici olabilen genetik değişikliklerin ayırt edilmesi moleküler tıbbın hızlı gelişen ajanlanndaki başarılandan biridir.
Karsinojenik etkiler açısından, sigara içimi ve çok daha az oranda diğer çevresel etkenlerin akciğer kanseri uçumundan sorumlu genetik değişikliklerin gelişmesinde esas. Suçlu etkenler olduğuna ilişkin güçlü kanıtlar vardır. Önce sigara içimi ile ilişkili kanıtlar verilecek sonra diğer daha az önemli etkenler hakkında kısa yorum yapılacaktır.
İstatistiksel, klinik ve deneysel kanıtların etkileyici bir şekildeki bütünlüğü, akciğer kanseri nedeni olarak sigara içimini suçlu çıkartmaktadır. İstatistiksel olarak akciğer kanserlerinin %90'ı aktif sigara içicilerinde ya da henüz yeni bırakmış kişilerde görülmektedir. Akciğer kanseri sıklığı ile sigara içme sıklığı arasında neredeyse lineer bir korelâsyon mevcuttur. Sigara içmeyenlere göre ağır sigara içiciliği alışkanlığı olanlarda (20 yıl 2 paket/gün) risk 60 kat fazladır. Nedeni tam anlaşılamamış olsa da kadınlar tütünün bu etkisine daha çok hassastır. Sigara içiminin kesilmesi ile zamanla risk düşse de hiçbir zaman hiç içmemiş birisinin düzeyine ulaşamamaktadır. Aslında akciğer kanseri oluşumuna zemin hazırlayan genetik değişiklikler daha önce sigara içen kişilerin bronş epiteli içinde yıllar boyunca kalıcı olabilir.
Pasif içicilerde ise (sigara kullanan yakını olanlarda) risk yenlere göre yaklaşık 2 kat artmıştır. Pipo ve puro içimi de daha hafif olsa da bir risk artışı oluşturmaktadır. Klinik kanıtlar büyük ölçüde sigara içme alışkanlığı olan kişilerin solunum yollanandaki epitelinde gösterilen progresif morfolojik değişikliklere dayanmaktadır. Bu ardışık değişiklikler en iyi skuarnöz hücreli karsinomlarda dökümante edilmiştir, ancak diğer histolojik alt tiplerde de gösterilebilir. Aslında sigaraya marufiyetin derecesi ile giderek kötüleşen epiteliyal değişikliklerin gelişimi arasında lineer bir korelâsyon vardır. Bu değişiklikler zararsız bazal hücre hiperplazisi ve skuamöz metaplaziden skuamöz displazi, karsinoma in situ ve invaziv kansere kadar değişmektedir. Akciğer kanserinin major histolojik tipleri arasında tütün içimi ile en güçlü birliktelik skuamo; ve küçük hücreli akciğer kanserlerinde gözlenmektedir.
Deneysel kanıtlar, her geçen yıl artsa da önemli bir bileşen eksiktir: bugüne kadar sigaraya maruz bırakılarak hiçbir hayvanda akciğer kanseri geliştirmek mümkün olmamıştır. Bununla birlikte sigara dumanı konsantresi politiklik hidrokarbonlar ve diğer mutajen ve karsinojenlerden çok zengindir. Deneysel modelin eksikliğine rağmen, sigara içimi ve akciğer kanseri arasındaki ilişkiyi gösteren kanıtlar zinciri her geçen gün büyümektedir. Diğer etkenler sigara ile birlikte veya kendi başlarına akciğer kanserlerinin gelişiminden sorumlu olabilirler; radyoaktif maddelerin bulunduğu maden ocağı madencilerinde, asbest işçilerinde, arsenik, krom, uranyum, nikel, vinil klor id ve hardal gazına maruz kalanlarda akciğer kanseri insidansında artış gözlenmektedir. Sigara içmeyenlerde asbeste maruz kalını akciğer kanserini S kat artmaktadır, Ağır sigara içimi olan ve asbeste maruz kalanlarda akciğer kanseri riski sigara içmeyen ve asbeste maruz kalmayanlara göre yaklaşık 55 kat artmaktadır.
Sigara içimi ve diğer çevresel etkenler akciğer kan serinin en önemli nedenleri olsalar da tütün içimi olan her kişi akciğer kanseri olmamaktadır. Kişilerde karsinojenlerin mutajenim etkilerini koşullayan genetik faktörlerin varlığı akciğer kanseri gelişiminde önemli bir olasılık gibi görünmektedir. Bazı kimyasal maddeler (prokarsinojenler) karsinojenlere dönüşrnek için P-4S0 monooksijenaz enzim sistemi aracılığı ile metabolik aktivasyona ihtiyaç duyarlar (Bölüm 6). P-4S0 genleri gibi spesifik genetik polimorfizrnleri içeren kişilerin sigara içimi ile oluşan prokarsinojenleri daha fazla metabolize etme kapasi tesinin artması ve akciğer kanseri riskinin artması akla yatkın bir düşüncedir. Benzer olarak, tütün ile ilişkili karsinojenlere maruziyet sonrası (mutajen duyarlı genotip) kan lenfositlerinde kromozomsal kınlamaların olması akciğer kanseri riskini kontrollere göre 10 kat artırmaktadır.
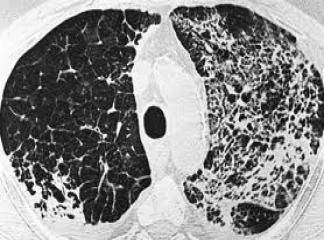
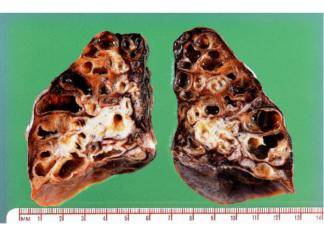
Morfoloji
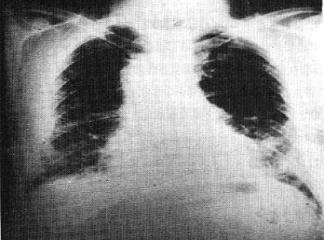
Akciğer karsinomları genelde küçük sert gri beyaz renkte mukozal lezyonlar şeklinde başlarlar. intraluminal kitle biçiminde, bronş mukozasını invaze ederler ya da büyük hacimli kitle yaparak bitişik akciğer parankimini itebilirler. Bazı büyük kitleler santral nekroza ya da fokal kanamaya bağlı olarak kavitasyona uğrarlar. Sonunda bu tümörler plevraya erişerek plevral kavite ve göğüs duvarını invaze eder ve komşu intratorasik yapılara yayılır. Daha uzak yayılımlar lenfatikler yada hematojen yol ile ortaya çıkabilir. Skuamöz hücreli karsinomlar erkeklerde kadınlardan daha sık olup sigara içme öyküsü ile yakın ilişkidedir. Bunların santralde major bir bronkusda çıkma eğilimleri vardır ve sonunda lokal hılar nodalara yayılırlar, fakat diğer histolojik tiplere göre toraksa dışına daha geç yayılırlar. Büyük lezyonlar kavitasyona neden olan santral nekroza uğrarlar. Karakteristik skuamöz hücreli karsinoma genelde daha önceden ortaya çıkan preneoplastik lezyonlar eşlik eder.
Bronşial epitelin daha sonra karsinoma insituya ilerleyen skuamöz metaplazi veya displazisi, sıklıkla skuamöz hücreli karsinom gelişiminden yıllar öncesinde gelişerek bu hastalığa öncüllük eder. Skuamöz metaplazi veya displazi bronşial epitelde oluştuktan sonra yıllar boyunca karsinoma in situ şeklinde kalabilir. Bu aşamada radyolojik olarak saptanamayan ve asemptomatik lezyonlarda Sinolojik balgam yaymaları, bronşial yıkama sıvıları yâda fırçalamalarında atipik hücreler saptanabilir. Sonunda küçük bir neoplazi semptomatik evreye ulaşır. Tümör major bronkusda lümeni tıkadığı zaman distalinde atelektazi ve infeksiyona neden olur. Aynı zamanda lezyon çevre akciğer yapılarını da invaze eder.
Histolojik olarak bu tümörler keratin incileri ve interselüler köprüleşmeler gösteren iyi diferansiyel skuamöz hücreli neoplazilerden sadece minimal skuamöz hücre özelliği olan az diferansiyel neoplazilere kadar değişirler. Adenokarsinomlar skuamöz hücreli tipte olduğu gibi santral lezyonlar olarak ortaya çıkabilir fakat genelde daha periferim yerleşimlidir. Çoğu periferim akciğer skorları zemininde gelişir ("skor karsinomları"). Bu birlikteliğin etiyolojik temeli açık olmamakla beraber bugünkü düşünceye göre skorlaşmanın tümöre neden olmaktan ziyade tümöre sekonder olarak geliştiği yönündedir.
Adenokarsinomlar kadınlarda ve sigara içmeyenlerde en sık görülen akciğer kanseri tipidir. Adenokarsinom genellikle diğer tiplerden daha yavaş büyür ve daha küçük kitleler oluşturur, fakat erken evrede metastaz yapma eğilimi vardır. Histolojik olarak asiler (Grand oluşturan), papeller, soliç tipleri gibi çeşitleri vardır. Adenokarsinom özelliğini kanıtlamak için soliç tipinde sıklıkla intrasellüler müsün yapımını özel boyalarla kanıtlamak gerekir. Rezece edilmiş adenokarsinomlasın proksimalindeki epitelde skuamöz metaplazi ve displazi odakları görülebilse de bunlar bu tümör için prekürsör lezyonlar değildir. Atipik adenomatöz hiperplazi (AAH) periferik adenokarsinomun olası prekürsör lezyonu olarak tanımlanmaktadır.
Mikroskopik olarak AAH iyi sınırlı epitel proliferasyon odağıdır. Epitel hücreleri Clara hücrelerine benzeyen küboid, alçak kolumnar hücreler ya da tip 2 pnömositlerden oluşur. Hücreler aşikar adenokarsinomdaki kadar olmasa da değişik derecelerde sitolojik atipi (nükleer hiperkromazi, pleomorfizm, belirgin nükleol) gösterirler. Genetik analizler AAH'nin lezyonlarının monoklonal olduğunu ve adenokarsinomlarda görülen moleküler sapmaların çoğunun AAH'de de görüldüğünü göstermektedir (örneğin KRAS mutasyonları).
Dünya sağlık örgütünün güncel akciğer tümörleri sı-nıflamasında bronşioloalveolar karsinomlar (BAK) adenokarsinomların alt tipi olarak alınmıştır. Bunlar akciğerin periferik kısımlarında tek bir nodül ya da daha sıklıkla birleşip bütünleşerek pnömoni benzeri konsolidasyon gösteren multiple diffüz nodüller olarak ortaya çıkar. Bakıların ana özellikleri var olan yapılar boyunca büyümeleri ve alveol çatısını korumalarıdır. Tümör hücreleri yapının iskeleti gibi görev yapan alveol septasında tek tabaka olarak büyürler. Neoplastik hücreler çit üzerine dizilen kelebeklere benzediği için buna "Iepidic" büyüme paterni denir. Tanım itibarı ile BAK alveoler yapıda yıkım veya adenokarsinomun özelliği olan desmoplazi ile birlikte stromal invazyon göstermez.
Bakıların müsinöz ve non müsinöz iki alt tipi vardır. Müsinöz tipinde sitoplâzmalarında mısın bulunan uzun kolumnar hücreler ve alveol içinde misin bulunur. Bazı invaziv akciğer adenokarsinomlarının kolondaki adenokarsinom sekansına benzer şekilde atipik adenomatöz hiperplazi-bronşioloalveolar karsinom-invaziv adenokarsinom safhalarını geçirerek geliştikleri sanılmaktadır. Bununla birlikte tüm adenokarsinomların bu biçimde ortaya çıkmadığının ve tüm BAK‘I arın kendi halinde bırakılıp tedavi edilmediğinde invaziv olabileceğinin vurgulanması önemlidir. Santralde lokalize skuamöz hücreli karsinomun ve küçük hücreli akciğer karsinomunun köken aldıkları hücreler bilinirken (skuamöz hücreli karsinom bronşlardaki meta plastik skuamöz epitelden, küçük hücreli karsinom akciğere özgü nöroendokrin hücrelerden), periferal adenokarsinomun hücre kökeni son zamanlara kadar bilinmiyordu.
Farelerde yapılan akciğer hasarlanma modeli çalışmalarında broşioloalveoler kanal kavşaklarında bronşioloalveolar kök hücre (BAKH) adı verilen multipotent hücre populasyonu tanımlanmıştır. Periferik akciğer hasarını takiben multipotent BAKH‘ ler yayılarak zedelenen alanda normalde bulunan hücre tiplerinin (Clara hücreleri ve alveolar hücreler) yerine geçerek epiteliyal dejenerasyonu kolaylaştırırlar. BAKH‘ lerin onkojenim olayların başlamasından etkilenerek (örneğin somatik K-RAS mutasyonu) normal kontrol noktalarından kaçabildiği ve sonuçta pulmoner adenokarsinom oluştuğu varsayılmaktadır.
Büyük hücreli karsinomlar küçük hücreli karsinomun sitolojik özelliklerini içermeyen ve Glandüler ya da skuamöz diferansiyasyon göstermeyen indiferansiye (ayrımlaşmamış) malign epiteliyal tümörlerdir. Hücreler tipik olarak büyük nükleustu, belirgin nükleolu ve orta miktarda sitoplâzmalıdır. Büyük hücreli karsinomlar ışık mikroskobu ile muhtemelen tanınamayacak kadar indiferansiye (ayrımlaşmamış) skuamöz hücre ya da adenokarsinomu temsil edebilirler. Bununla birlikte ultrastrüktürel olarak minimal Glandüler ya da skuamöz diferansiyasyon sıktır.
Küçük hücreli akciğer karsinomları genellikle açık gri renkte, akciğer parankimini yayılan santral lokalizasyonlu kitleler olup hılar ve mediastinal lenf nodlarına erken i m gösterirler. Bu kanserler yuvarlak iğsi şekilli, dar siolazmalı ve ince granüller kromatinli tümör hücrelerinden Mitoz sık görülür. Neoplastik hücreler uçuk olarak adlandırılmalarına rağmen lenfositlerin genellikle iki katı büyüklüğündedir. Nekroz her zaman vardır ve yaygın olabilir. Tümör hücreleri belirgin olarak kırılgan olup küçük biyopsi örneklerinde sıklıkla parçalanma ve "ezilme artefaktı" gösterir. Küçük hücreli karsinomların bir diğer özelliği en iyi sitolojik yaymalarda görülen dar sitoplâzmalı tümör hücrelerinin sıkıca yan yana gelmesiyle oluşan nükleer holding‘dir. Bu tümörler akciğerin nöroendokrin hücrelerinden köken alırlar bu nedenle çeşitli nöroendokrin belirteçler salgılarlar. Ek olarak polipeptid hormonlar için bir kaynak oldukları için para neoplastik sendromlara neden olurlar.
Kombine paternler daha fazla yorum gerektirmez fakat Bronkojenik karsinomların azımsanmayacak bir kısmının birden fazla (bazen çok sayıda) diferansiyasyon gösterdiği belirtilmelidir (Tablo 13-8). Bu durum tüm bu tümörlerin multi potansiyel kök hücreden köken aldığını düşündürmektedir. Tüm bu neoplaziler için karina, media sten, boyun (skalan nodalar), klavikular bölgedeki ardıl lenf nodu zincirinde ve erken ya da geç uzak metastazlar saptanabilir. Sol supraklavikular nod tutulumu (Virchow nodu) özellikle karakteristik olup bazen gizli primer bir tümörün varlığına dikkat çeker. Bu kanserler ilerlerse sıklıkla perikardial yada plevral aralığa yayılarak inflamasyon ve effüzyona neden olurlar. Superiyor vena cavayı basıya uğratır veya infiltre ederlerse venöz konjesyona veya tam gelişmiş vena cava sendromuna neden olurlar.
Apikal neoplaziler brakial veya servikal sempatik pleksusu invaze ederek ulnar sinir dağılım yerlerinde şiddetli ağrıya veya Korner sendromuna neden olabilir (ipsilateral enoftalmus, ptosis, miyosis ve anhidrosis). Bu gibi apikal neoplaziler bazen Pancoast tümörler olarak adlandırılırlar ve klinik bulgularla birlikteliğine Pancoast sendromu denir. Pancoast tümörüne sıklıkla birinci, ikinci kosta ve bazen torasik vertebra yıkımı eşlik eder. Diğer kanserler gibi tümör-lenf nodu-metastaz (TNM) sınıflaması yapılarak primer tümörün boyut ve yayılma durumu gösterilir. Skuamöz hücreli karsinom genellikle santral (hiler) kitle olarak başlar ve periferik parankime doğru büyür. Skuamöz hücreli karsinomiarda intrapulmoner yayılım esnasında kaviter nekroz nadir değildir.
Klinik Gidiş
Akciğer karsinomdan sessiz ve sinsi gidiş gösterirler ve semptomlar oluşturmadan önce sıklıkla cerrahi olarak çıkanlaşmayacak şekilde yayılmışlardır. Bazı durumlarda kronik öksürük ve balgam çıkarma hala lokalize ve cerrahi olarak çıkarılabilir bir hastalık için dikkat çekici olabilir. Ses kısıklığı, göğüs ağrısı, superior vena kava sendromu, perikardial ve plevral effüzyon, veya segmental atelektaziler veya pnömoniler ortaya çıktığı zaman prognoz zaten kötüleşmiştir. Sıklıkla, tümör beyine (mentol ve nörolojik değişiklikler), karaciğere (hepatomegali) veya kemiklere (ağrı) meta statik yayılım göstererek semptomlar oluşturabilir. Adrenaller meta statik hastalıkta oblitere olsa da adrenal yetmezlik (Addison hastalığı) nadirdir. Çünkü adrenal fonksiyonları devam ettirecek hormon sekresyonunu sağlayabilecek kadar kortikal hücre genellikle kalır.
Genelde NSCLC, SCLC‘ YE göre daha iyi prognozudur. NSCLC (skuamöz hücreli karsinomlar veya aderıo karsinomlar) metastaz ve lokal yayılımdan önce tanı alabilirlerse lobektomi veya pnömonektomi ile kür şansı vardır. Buna karşın primer tümör henüz küçük ve lokalize iken bile, SCLC tanı aldığında yayılmıştır. Bu nedenle cerrahi eksizyon uygulanabilir tedavi değildir. Kemoterapiye duyarlıdır ancak kaçınılmaz olarak rekürrens gösterir. Tedaviye rağmen ortalama yaşam ıyıldır.
Akciğer kanserli hastaların %3-1O'unda klinik olarak para neoplastik sendrom bulguları ortaya çıkar. Bunlar: (1) paratroid hormon-ilişkili peptid sekresyonuna bağlı olarak hiperkalsemi gelişimi (osteolitik lezyonlar hiperkalsemiye neden olabilir, fakat bu para neoplastik sendrom olmayabilir [Bölüm 6]) ; (2) Cushing sendromu (adrenokortikotropik hormon sekresyon artışı); (3) uygunsuz antidiüretik hormon sekresyonu sendromu; (4)
Miyastenik sendrom, periferik nöropati ve polimiyozit gibi nöromüsküler sendromlar; (5) çomak parmak ve hipertrofim pulmoner osteoartropati; (6) gezici tromboflebit, nonbakteriel endokardit, dissemine intravasküler koagülasyon gibi hematolojik gösterimlerdir. Kalsitonin ve diğer ektopik hormonların sekresyonu incelemelerle gösterilebilir ancak bu ürünler genellikle farklı sendromları uyarmaz. Hiperkalsemi en sık olarak skuamöz hücreli kanserde görülür. Hematolojik sendromlar adenokarsinomlarla birliktelik gösterir. Geriye kalan sendromlar ise küçük hücreli akciğer kanseri ile birliktelik gösterirler ancak istisnalar da vardır.